
Технологии ионного обмена в современной водоподготовке успешно дополняют такие процессы, как дистилляция, обратноосмотическая фильтрация, адсорбция и фильтрация. Основная область применения ионитов в настоящее время – селективное удаление из воды различных ионов, декарбонизация, удаление высокомолекулярной органики, умягчение и обессоливание воды в процессах водоподготовки.
Ионообменные смолы представляют собой синтетические высокомолекулярные вещества с функциональными ионными группами, способными к обратимому обмену ионов в эквивалентном количестве.
По знаку заряда обменивающихся противоионов иониты подразделяются на:
аниониты, обменивающие отрицательно заряженные ионы;
Иониты также дополнительно подразделяются на 4 функциональных группы:
Сильноосновные аниониты – обменивающие анионы любой степени диссоциации в растворах при любых значениях рН
Слабоосновные аниониты – способные к обмену анионов из растворов кислот при рН 1-6
Сильнокислотные катиониты – обменивающие катионы в растворах при любых значениях рН
Слабокислотные катиониты – способные к обмену катионов в щелочных средах при рН> 7
ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ИОНИТОВ
Обменная емкость
Для количественной характеристики ионообменных свойств ионитов применяют следующие величины: полная и рабочая обменная ёмкость, выражающиеся в мг-экв\л.
Полная обменная емкость определяется числом функциональных групп, потенциально способных к ионному обмену в единице массы ионита.
Рабочая обменная емкость – важнейший показатель в процессах водоподготовки. В реальных условиях многократного применения ионита в цикле сорбции-регенерации обменная емкость используется не полностью, а лишь частично. Степень использования определяется методом регенерации и расходом регенерирующего агента, временем контакта ионита с регенерирующим агентом, концентрацией солей, рН, конструкцией и гидродинамикой используемого аппарата.
Процесс очистки воды прекращают при определенной остаточной концентрации лимитирующего иона в фильтрате и, как правило, задолго до полного исчерпания ионитом своей обменной ёмкости.
Селективность
Под селективностью понимают способность ионита избирательно сорбировать ионы из растворов сложного состава. Селективность определяется типом ионогенных групп, числом поперечных связей матрицы ионита, размером пор и концентрацией противоионов в растворе.
Как правило, селективность ионитов возрастает с увеличением заряда противоиона, а среди ионов с одним и тем же зарядом - с увеличением атомного веса. Т.е., чем тяжелее противоион и чем выше его заряд, тем большую селективность проявляет к нему ионит.
Типичный ряд селективности катионита:
H+ < Na+ < K+ < Cd2+ < Cs+ Ag+ < Mn2+ 2+ < Zn2+ < Cu2+ < Ni2+ < Co2+ < Ca2+ < Sr2+ < Al3+ < Fe3+
Типичный ряд селективности анионита:
OH- ~ F- < HCO3- < Cl- < NO3- < PO43- < CrO42- < SO42-
Обратимостью ионного обмена обусловлено важнейшее свойство ионитов - их способность к регенерации после насыщения ионами, удаляемыми из воды, путем промывки растворами кислот (для катионитов) или растворами щелочей (для анионитов). Например, двухзарядные противоионы вытесняются из ионита однозарядными противоионами при контакте с регенерационным раствором, содержащим однозарядные противоионы в высокой концентрации.
Осмотическая стабильность.
При изменении характеристик среды (солесодержание, рН раствора и т.д.) происходит разрушение зёрен ионитов вследствие изменения объёма зерна, который из-за осмотического эффекта в концентрированных растворах меньше, чем в разбавленных.
При этом, внешний слой сжимается или расширяется быстрее, чем ядро зерна – возникают большие внутренние напряжения и происходит откалывание верхнего слоя или раскалывание всего зерна.
Это явление называется «осмотическим шоком». Каждый ионит способен выдерживать определенное число циклов таких изменений характеристик среды.
Данное значение называется осмотической прочностью или стабильностью ионита.
Температурная устойчивость
Температурная устойчивость катионитов выше, чем анионитов. Слабокислотные катиониты работоспособны при температуре до 130 ° С, сильнокислотные катиониты работоспособны до температуры 100–120 ° С, а большинство анионитов – не выше 60 – 80 ° С.
Фракционный состав
На сегодняшний день наиболее распространены синтетические иониты моносферного типа, имеющие более высокую обменную емкость, осмотическую и механическую стабильность, обладающие очень малым разбросом размеров и низким коэффициентом неоднородности.
ТЕХНОЛОГИИ ИОНООБМЕННОЙ ФИЛЬТРАЦИИ.
Объём заполнения ионитом ионообменного фильтра в традиционных системах должен находиться в пределах 60-65% от полного объёма фильтра для обеспечения необходимого свободного пространства при расширении слоя загрузки – «эффект псевдоожиженного слоя».
Однако современные разработки – технологии «зажатого слоя» UPCORE, PUROPACK и SCHWEBEBETT (а также их родственные модификации типа UPFLOW и AMBERPACK) позволяют радикально уменьшить величину необходимого свободного пространства, тем самым увеличив объём ионита до уровня 80-90% от полного объёма фильтра при снижении общего количества регенераций.
Основные отличительные особенности применяемых технологий ионообменной фильтрации:
- Подача воды на фильтрацию «сверху-вниз».
Подача регенерационного раствора «сверху-вниз» стандартное решение - Подача воды на фильтрацию «снизу-вверх».
Подача регенерационного раствора «сверху-вниз» технология PUROPACK - Подача воды на фильтрацию «сверху-вниз».
Подача регенерационного раствора «снизу-вверх» технологии UPCORE, SCHWEBEBETT
Технологии PUROPACK, UPCORE и SCHWEBEBETT имеют между собой определённые конструктивные и технологические отличия, однако все относятся к системам с «зажатым слоем», отличающимся высоким качеством фильтрата, высоким объёмом загрузки, сниженными эксплуатационными расходами (вода на собственные нужды, расход регенеранта)
NA-КАТИОНИРОВАНИЕ.
Процесс применяется для умягчения воды путем фильтрования ее через загрузку катионита в Na-форме.
В реализуемом механизме ионного обмена ионы Ca2+ и Mg2+, обуславливающие общую жесткость исходной воды, обмениваются на эквивалентное количество ионов Na+.
2RNa + Ca2+ → R2Ca + 2Na+
2RNa + Mg2+→ R2Mg + 2Na+
Остаточная жёсткость фильтрата после Na-катионирования различной архитектуры может быть получена при надлежащих условиях регенерации катионита на уровне 0.005 – 0.01 мг-экв\л. Анионный состав фильтрата после Na-катионирования остаётся неизменным, что объясняется реакцией:
Ca(HCO3)2 + 2RNa → R2Ca + 2NaHCO3
Однако, необходимо помнить, что далее гидрокарбонат натрия при определённых условиях переходит в гидроксид натрия, который далее инициирует щёлочную коррозию:
2NaHCO3 + H2O → Na2CO3 + CO2 + H2O
Na2CO3 + H2O → 2NaOH + CO2
Недостатки способа Na-катионирования:
- неизменность величины общей щелочности в фильтрате, что ограничивает применение метода подготовки воды в энергетике только котлами низкого и среднего давления
- увеличение общего солесодержания фильтрата, что связано с эквивалентностью обмена и большей эквивалентной массой Na+ (23 ед.) в сравнении с массой удаляемых Ca2+ (20 ед.) и Mg2+ (12 ед.)
Н-КАТИОНИРОВАНИЕ
Метод H-катионирования предназначается для удаления катионов с заменой их на ионы водорода.
Механизм ионного обмена при H-катионировании сильнокислотным катионитом:
2RH + Ca(HCO3)2 → R2Ca + 2H2O + 2CO2
2RH + Mg(HCO3)2 → R2Mg + 2H2O + 2CO2
2RH + CaCI2 → R2Ca + 2HCI
2RH + MgSO4 → R2Mg + H2SO4
HR + NaCI → RNa + HCI
2RH + Na2SO4 → 2RNa + H2SO4
Процесс сорбции катионов Ca2+, Mg2+ и Na+ сильнокислотным катионитом осуществляется в соответствие с расположением этих ионов в ряду селективности, поэтому в слое H-катионита по ходу движения исходной воды располагается сначала зона поглощения Ca2+, ниже располагается зона Mg2+ и далее - Na+.
Эти три зоны по мере истощения H-катионита смещаются одна за другой по направлению движения воды к нижней границе слоя катионита.
К моменту прекращения поглощения иона Na+ начинается обмен в катионите ионов Ca2+ и Mg2+ исходной воды на сорбированный катионитом ион Na+ до его полного вытеснения.
Началом исчерпания обменной ёмкости ионита является обнаружение в фильтрате проскока иона Na+.
Вывод фильтра на регенерацию осуществляется по наступлению проскока ионов Na+ или ионов Ca2+ и Mg2+ – в зависимости от технологической схемы его использования.
Механизм ионного обмена при Н-катионировании слабокислотным катионитом:
Слабокислотный катионит удаляет все ионы Ca2+ и Mg2+, связанные с бикарбонатами.
2RH + Ca(HCO3)2 → R2Ca + 2H2O + 2CO2
2RH + Mg(HCO3)2 → R2Mg + 2H2O + 2CO2
Вытесняемый катионами жёсткости водородный катион образует с анионом бикарбоната очень слабую угольную кислоту, которая препятствует созданию очень низких значений pH в зоне ионного обмена, и тем самым поддерживает слабокислотный катионит в ионизованном состоянии только до тех пор, пока в воде присутствуют бикарбонат-ионы (или ионы других очень слабых кислот).
Катионы жёсткости, связанные в исходной воде с анионами сильных минеральных кислот, слабокислотным катионитом не удаляются, т.к. образуемые в процессе ионного обмена сильные кислоты препятствуют ионизации слабокислотного катионита.
ОН-АНИОНИРОВАНИЕ.
Метод ОН-анионирования воды предназначается для замены анионов на ионы гидроксила.
При сочетании ОН-анионирования с Н-катионированием происходит удаление из воды как анионов, так и катионов в обмен на ионы ОН- и Н+, т.е. осуществляется химическое (ионообменное) обессоливание воды.
При фильтровании через слой анионита осуществляется сорбция анионов согласно реакциям:
ROH + HCl → RCl + H2O
2ROH + H2SO4 → R2SO4 + H2O
ROH + HNO3 → RNO3 + H2O
Высокое значение pH в зоне обмена на анионите способствует диссоциации слабых кислот H2CO3 и H2SiO3 и переводу их в ионизированное состояние, поэтому они также могут участвовать в реакциях анионного обмена, но лишь при использовании сильноосновных анионитов.
ROH + (H+ + HCO3-) → RHCO3 + H2O
ROH + (H+ + HSiO3-) → RHSiO3 + H2O
С учётом значений обменных ёмкостей слабоосновных и сильноосновных анионитов, а также способности только последних сорбировать анионы слабых кислот, схемы химического обессоливания обычно включают две ступени анионирования: на первой ступени в фильтры загружается слабоосновный анионит, удаляющие ионы SO42- и Cl-; на второй ступени в фильтры загружается сильноосновный анионит, предназначенный часто для удаления ионов HSiO3- .
РЕГЕНЕРАЦИЯ ИОНООБМЕННЫХ СМОЛ.
На сегодняшний день основной задачей в вопросе технологии регенерации ионообменных смол является увеличение рабочей обменной ёмкости ионитов при снижении эксплуатационных расходов.
Особенности регенерации катионита в Na-форме.
Регенерацию истощённого катионита проводят 8 - 10%-ным раствором NaCl. Типовой расход NaCI на регенерацию принимают в пределах 140 - 170 г/г-экв, однако при таком расходе рабочая обменная ёмкость не достигает значения полной.
Увеличение расхода NaCI при регенерации обеспечивает эффект прироста обменной ёмкости, однако расход NaCI свыше 300 г\г-экв экономически и экологически нецелесообразен.
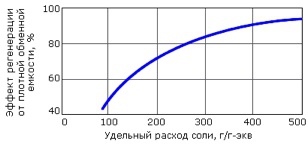
Влияние расхода NaCI на эффект регенерации катионита
Линейная скорость пропуска регенерационного раствора ограничивают пределами 5 - 8 м/ч для обеспечения необходимой продолжительности контакта раствора NaCI с катионитом.
Линейная скорость ниже 5.0 м/ч не используется по причине возникновения «туннельного эффекта».
Особенности регенерации катионита в Н-форме.
При выборе кислоты для восстановления рабочей ёмкости катионита следует отдавать предпочтение соляной кислоте, что позволяет избежать «гипсования» ионита - выпадения солей кальция в слое смолы в случае применения для регенерации раствора H2SO4.
Регенерацию истощённого катионита проводят:
0.6 – 1.5 %-ным раствором H2SO4.
2.0 – 6.0 %-ным раствором HCI
В случае применения H2SO4 необходимо соблюдать концентрацию кислоты при регенерации на уровне – менее 0.8%.
Дополнительно при применении H2SO4 можно использовать «пошаговую» регенерацию. Это позволяет несколько уменьшить объёмы используемого регенеранта.
Максимальная концентрация H2SO4 при «пошаговой» регенерации составляет 1,5%. Такая высокая концентрация кислоты должна быть использована во второй (заключительной) стадии при «пошаговой» регенерации.
Особенности регенерации анионитов.
Регенерация анионитных фильтров в зависимости от типа и назначения анионита – сильноосновные или слабоосновные аниониты; для схем обессоливания или для удаления высокомолекулярной органики, применение различных функциональных групп – может производится различными реагентами:
- 2-8% раствором NaOH
- 8-10% раствором NaCI
- 3-4% раствором NH3
- 6% раствором NaHCO3
В качестве воды для обеспечения процесса регенерации используется вода, прошедшая катионитный фильтр или обессоленная вода.
НЕДОСТАТКИ ТЕХНОЛОГИЙ ИОННОГО ОБМЕНА.
Основные недостатки ионообменной технологии связаны с применением для восстановления обменной ёмкости ионитов определённых количеств растворов щёлочи и кислоты. Это в свою очередь приводит к необходимости наличия сложного реагентного хозяйства.
Компания Филтрокс производит установки ионного обмена серии FIE в стандартном и индивидуальном исполнении.
КОМПЛЕКТАЦИЯ ТИПОВЫХ УСТАНОВОК ИОННОГО ОБМЕНА СЕРИИ FIE.
- корпуса фильтров в проектном количестве:
технология – прямоток или противоток
исполнение - одинарное, дуплекс, триплекс, квадро
диаметр - от 250 мм до 3400 мм
материал изготовления - углеродистая сталь с антикоррозионным покрытием, нерж. сталь или композитные материалы - пластик и стекловолокно
рабочее давление - от 4 до 20 атм
- дренажно-распределительные системы «верх-низ» внутри корпуса фильтра
материал изготовления - нерж. сталь или пластик
модификации – щелевые колпачки, лучевые одно- и двухъярусные системы, щелевые стаканы
- ионообменная фильтрующая загрузка
исполнение - катионит или анионит
- запорно-регулировочная арматура
модификации – клапана с пневмо-, гидро- или электрическим приводом под управлением центрального контроллера, автоматические многоходовые клапана управления
- трубопроводная обвязка
материал изготовления - нержавеющая сталь или пластик - ПВХ, ПП, ПЭ
- контрольно-измерительные приборы
комплектация - манометры, рН-метры, ORP-метры, датчики давления, специализированные приборы «on-line» аналитического химконтроля
- узел проведения регенерации
- опорной рамная конструкция
материал изготовления - нерж. сталь или углеродистая сталь с антикоррозийным покрытием
Технические спецификации на ионнообменные смолы смотреть здесь
